
Misura le radiazioni emesse da un materiale, come il piombo, identificando quali e quanti elementi radioattivi sono presenti al suo interno.
Lo spettrometro alfa, come suggerisce il nome, è in grado di rivelare le radiazioni di tipo alfa. Queste vengono emesse da elementi che “decadono”, cioè passano da una condizione instabile a una più stabile, rilasciando due neutroni e due protoni. Lo spettrometro permette di scoprire quale elemento radioattivo ha prodotto le emissioni e quanto è abbondante. Il piombo emette radiazione alfa in quantità variabile, in base all’età del piombo stesso.
Alcuni elementi, tra cui tutti quelli più pesanti del piombo, sono radionuclidi, cioè subiscono decadimenti radioattivi. In questi processi, un nucleo inizialmente instabile perde energia attraverso l’emissione di una o più particelle diverse. A seconda di quali particelle sono emesse, i decadimenti radioattivi sono generalmente chiamati di tipo alfa, beta e gamma. Nel decadimento beta (e le sue varianti, come la cattura elettronica e il decadimento beta inverso) un nucleo cambia natura e ciò può avvenire in due modi diversi. Nel primo si ha la trasformazione di un neutrone in protone, accompagnata dall’emissione di un neutrino e un elettrone; nel secondo è invece il protone a trasformarsi in neutrone, emettendo questa volta un antineutrino e un positrone, le particelle di antimateria corrispondenti a neutrino ed elettrone.
Molto spesso a seguito del decadimento beta, il nucleo dell’atomo finale non è “stabile” e subisce un “riassestamento energetico” che culmina con l’emissione di raggi gamma, fotoni di altissima energia, 10-100 volte più energetici dei raggi X usati nelle lastre. Nel decadimento alfa, infine, la trasformazione comporta l’emissione di un nucleo di elio, una particella carica composta da due neutroni e due protoni, chiamata anche particella alfa. A differenza degli altri decadimenti, la particella alfa si ferma in pochi centimetri di aria, anche se possiede energia maggiore dei raggi gamma. Ogni elemento radioattivo lascia la sua particolare “firma”, legata al tipo di radiazione e alla sua energia. Perciò se si ritrova questa firma in un materiale si può concludere che l’elemento (radioattivo) è presente. In alcuni materiali, la presenza o meno di una firma del genere dipende dall’età del materiale stesso. Il piombo particolarmente attivo ad esempio, perde nel tempo tutta la sua radioattività iniziale ed è un ottimo materiale per schermare esperimenti come CUORE dalle radiazioni ambientali.
Lo strumento specializzato nell’identificare all’interno di un materiale gli elementi radioattivi che subiscono decadimento di tipo alfa si chiama spettrometro alfa. Le emissioni alfa hanno la caratteristica di essere assorbite molto velocemente, scomparendo in poco tempo. Infatti, a causa della loro carica (2+, data dalla presenza di due protoni) e della grande massa, i nuclei di elio interagiscono molto per mezzo della forza elettromagnetica con la materia che attraversano, venendo assorbiti da questa molto facilmente: le radiazioni alfa possono essere assorbite da un semplice foglio di carta oppure dallo strato esterno della pelle umana dello spessore di poche cellule. Per poter rivelare queste particelle gli spettrometri alfa utilizzano solitamente materiali cosiddetti semiconduttori, ad esempio cristalli di silicio. Le proprietà di tali cristalli fanno sì che al loro interno si possa creare una zona in cui il passaggio di una radiazione anche molto debole genera un flusso di corrente elettrica misurabile. Vediamo più in dettaglio come.
Un semiconduttore può essere “drogato”, cioè per così dire sporcato con delle impurità, in modo tale che al suo interno vi sia una certa quantità di elettroni in eccesso (semiconduttore di tipo n) o in difetto (semiconduttore di tipo p). Nel primo caso gli elettroni trasportano carica negativa, mentre nel secondo le “lacune” create dalla loro assenza si comportano a tutti gli effetti come trasportatori di carica positiva. Connettendo due sottili strati p e n, si crea all’interfaccia tra le due superfici una zona chiamata giunzione p-n, una porzione di spazio che, con l’applicazione di una tensione elettrica, può essere resa neutra e “impermeabile” al passaggio di cariche da una parte all’altra del semiconduttore. Quando ciò avviene, in questa zona si forma un campo elettrico che espelle immediatamente qualsiasi carica che si generi al suo interno. In queste condizioni, quando una particella carica esterna attraversa questo spazio, interagisce con gli elettroni del materiale ionizzandoli – estraendoli dai loro atomi –, creando all’interno della giunzione centinaia di migliaia di coppie elettrone-lacuna che vengono subito espulse, generando un impulso di corrente misurabile dal rivelatore. Dall’intensità dell’impulso si ricava l’energia della particella – la radiazione che vogliamo identificare – che lo ha generato. Questo è il principio di funzionamento che sfrutta uno spettrometro alfa. A livello pratico, in questi strumenti un sottile strato opportunamente trattato di campione del materiale da analizzare è posto in prossimità del rivelatore, all’interno di un volume in cui viene praticato il vuoto.
Il vuoto è essenziale poiché le radiazioni alfa potrebbero essere assorbite dall’aria prima di raggiungere il rivelatore. Quest’ultimo è accoppiato a un circuito che amplifica il segnale elettrico (poiché l’energia depositata dalla radiazione alfa è tipicamente molto piccola) e a un software in grado di elaborare questi segnali, ossia di discriminarli nel tempo (possono essere molto ravvicinati) e di calcolarne l’energia. Per quanto complesso, uno spettrometro alfa ha dimensioni molto ridotte, più o meno la metà di un forno a microonde (Fig.1).

Fig.1 Uno spettrometro alfa, composto di tre moduli indipendenti (Crediti immagine: Canberra Industries).
Il risultato finale dell’analisi di un materiale è lo spettro delle radiazioni emesse: un grafico in cui sull’asse orizzontale è riportata l’energia misurata e su quello verticale il numero di particelle che hanno depositato quella determinata energia (Fig. 2). Poiché ogni elemento radioattivo emette radiazione di una certa energia, di cui conosciamo il valore, dall’analisi dello spettro si può capire quali elementi radioattivi sono presenti nel campione. Se ad esempio si sa che un dato elemento emette radiazione di energia X, per capire se è presente nel campione basterà andare a vedere se in corrispondenza del valore X c’è un picco nello spettro. Inoltre, più il picco è alto, maggiore sarà la quantità dell’elemento radioattivo presente nel materiale. La spettroscopia alfa è una tecnica largamente usata per testare le proprietà di materiali, fare analisi geologiche o mineralogiche e monitorare la radioattività ambientale.
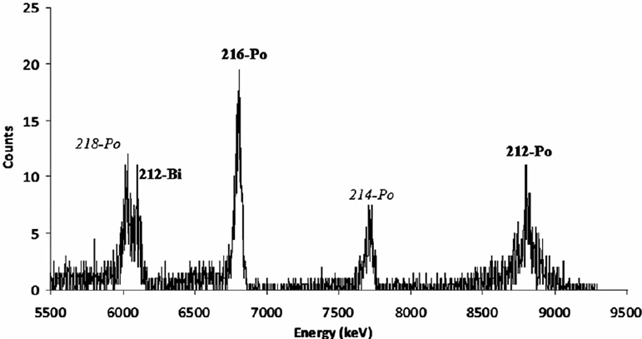
Fig.2 Esempio di uno spettro alfa. Sull'asse x i valori dell'energia rilasciata e sull'asse y il numero di radiazioni conteggiate. I picchi corrispondono a radiazioni emesse da isotopi radioattivi del polonio (Po) e del bismuto (Bi) (Crediti immagine: da Buompane et al. Radiation Protection Dosimetry, 2014, p. 1-4).
Lo spettrometro alfa non è l’unico strumento usato per misurare radiazioni. Uno molto conosciuto e particolarmente semplice è il contatore Geiger, che emette un particolare suono simile a un “crack” ogni volta che rivela una radiazione. Un contatore Geiger è essenzialmente costituito da un tubo riempito di un gas a cui è applicato un campo elettrico. Quando una radiazione entra nel tubo, ionizza gli elettroni del gas che vengono accelerati verso un elettrodo positivo (anodo) eccitando e ionizzando altri elettroni in un effetto valanga. La valanga è molto breve e crea un intenso impulso di corrente che viene rivelato e si traduce in un conteggio. Questo strumento – molto più economico di uno spettrometro alfa – è in grado di rivelare radiazione alfa, beta e gamma, ma si limita a contare, senza dare alcuna informazione sull’energia delle radiazioni che rivela (non produce alcuno spettro). A differenza dello spettrometro alfa, il contatore Geiger dà una indicazione della quantità di radiazione emessa, ma non della sua natura e quindi non permette di risalire a quali elementi l’abbiano generata.
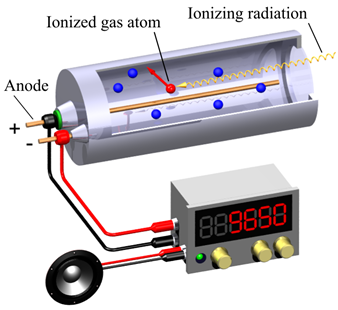
Fig.3 Rappresentazione grafica di un contatore Geiger. La radiazione (ionizing radiation) entra nel tubo ionizzando gli atomi del gas (ionized gas atom), che accelerati dal campo elettrico producono un impulso elettrico per effetto valanga. L'impulso si traduce in un conteggio sul display dello strumento, e in un rumore simile a un crack per mezzo di un piccolo amplificatore (Crediti immagine: Wikimedia Commons).

Scopri gli esperimenti e aiuta l'alieno a tornare a casa!
Gioca ora